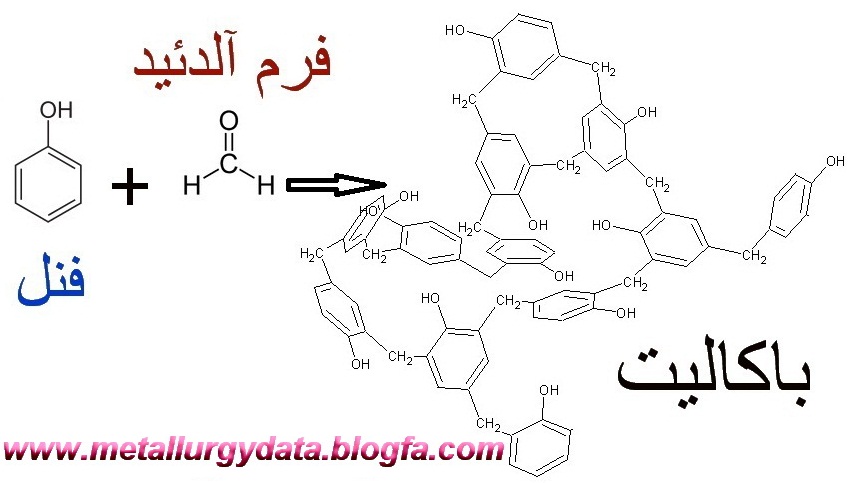
باکالیت
یک مادهٔ گرماسخت و یک ترکیب مصنوعی از رزین است که با باله هایی مانند
خاکهچوب و پنبهٔ نسوز ساخته میشود تا استحکام آن بالا رود. باکلیت ممکن
است به شکل میلهای، لولهای، تخته یا ورق ساخته شود و قابلیت سابخوردن،
بریدهشده، سوراخشدن، ارهشدن و حکاکیشدن و پرداخت را داراست. باکلیت از
کربولیکاسید (فنول) و فرمالدهاید به دست میآید و مادهای ارزانقیمت است
که میتواند در رنگهای مختلف ساخته شود.و به عنوان عایق حرارتی و الکتریکی
به کار رود.
باکالیت
ترکیبی اکسیدپذیر است و در طی چند سال رنگ بیرونی آن تغییر خواهد کرد که
اغلب میتوان با استفاده از سنباده مشاهده کرد که رنگ داخلی آن متفاوت است.
باکالیتهای سفید رفتهرفته کرمرنگ؛ بنفش کمرنگ، قهوهای؛ فیروزهای،
سبز؛ و صورتی به نارنجی تبدیل میشوند. این پدیده معمولاً در برابر نور
آفتاب یا تماس با مواد شیمیایی همچون خوشبوکنندهها، افشانههای مو و مواد
آرایشی رخ میدهد.
رنگها
باکالیتهای
تکرنگ در تقریباً ۱۰۰ رنگ متفاوت تولید میشوند. باکالیتها را میتوان
با ترکیبی از این رنگها و به صورت کدر، نیمشفاف یا شفاف ساخت.
تشخیص از پلاستیک
از
آنجا انواع مختلف فنولیکرزین با نام باکالیت شناخته میشوند، تشخیص
باکلیت حقیقی کمی دشوار است که با چند آزمایش ساده از جمله بررسی ظرافتهای
دستی (در جواهرات) و وجود لایهٔ اکسید میتوان آن را از پلاستیک تشخیص
داد. با کشیدن پارچهٔ نخی آغشته به موارد پاککنندهٔ خاص روی باکالیت اصل
لکههای عاجی و زرد کمرنگ روی پارچه باقی میماند که از ویژگیهای باکالیت
است و پلاستیکها چنین اثری ندارند یا اینکه لکهشان همرنگ پلاستیک خواهد
بود. این روش تقریباً در همهٔ باکلیتها به جز باکلیتهایی که به تازگی
پرداخت شدهاند و زنگار رویشان از بین رفته است، یا باکلیتهای قرمز و سیاه
که گاهی نتایج گیجکننده میدهند، قابل استفاده است.
فنول
یکی
از ترکیبات ساده آلی بوده که از اتصال یک گروه هیدروکسیل و یک حلقه بنزنی
تشکیل می شود.فنول با فرمول(C۶H۵OH) با نامهای هیدروکسی بنزن(hydroxyl
benzene) وکربولیک اسید (carbolic acid) نیز شناخته می شود.فنول خالص جامدی
سفید رنگ با دمای ذوب ۴۲°C یا ۱۰۸°F است.فنول به طور معمول قابل انحلال
در آب میباشد و خاصیت اسیدی ضعیفی دارد (pKa=9.9).فنول به عنوان یک گند
زدا استفاده می شود.فنول با غلظت بالا میتواند باعث سوختگی پوست
شود.ترکیباتی که در آن بیش از یک گروه هیدروکسیل متصل به حلقه بنزن باشد را
ترکیبات پلی هیدریک فنول(poly hydric phenols)می نامند.فنول یکی از
ترکیبات مهم آلی مورد استفاده در صنعت است.فنول در بسیاری از صنایع به
عنوان ماده اولیه کاربرد دارد.برخی از موادی که از این ماده تولید می شوند
عبارتند از: نایلون، شوینده ها، افرودنیهای بنزین، آسپرین، پلی اورتان،
رنگها، علف کشها، نرم کننده ها، ضد اکسنده ها، روغنهای روان کننده، قارچ
کش ها.
فرمالدئید
گازی
با بوی تند است. این ترکیب سادهترین عضو گروه آلدئیدها بوده ، فرمول
شیمیایی آن HCHO است. فرمالدئید اولین بار توسط دانشمند روسی به نام
"الکساندر باتلر" در 1859 کشف شد. این گاز بهآسانی از احتراق ناقص ترکیبات
حاوی کربن ایجاد میشود. در دود حاصل از آتشسوزی جنگلها ، حجم زیادی از
فرمالدئید وارد جو میشود. به غیر از این ، دود حاصل از اگزوز اتومبیلها و
دود سیگار هم دارای مقادیری فرمالدئید هستند.
فرمالدئید بطور طبیعی در
اتمسفر از واکنش اکسیژن با متان و سایر هیدروکربنها در اثر نور خورشید حاصل
میشود. همچنین از فرآیند متابولیسم برخی از هیدروکربنها هم مقدار اندکی
فرمالدئید تولید میشود.
خواص فرمالدئید
فرمالدئید با اینکه در
دمای اتاق به صورت گاز است، اما در آب به خوبی حل میشود. فرمالدئید معمولا
به صورت محلول آبی 37 درصد به نام فرمالین عرضه میشود. فرمالدئید در آب ،
پلیمریزه شده ، شامل مونومرهای کوچک HCHO متصل به هم است. معمولا فرمالین
دارای درصد اندکی متانول برای محدود کردن پلیمریزاسیون است. فرمالدئید
خواصی مانند سایر آلدهیدها دارد. با این تفاوت که معمولا واکنش پذیرتر از
سایر آلدئیدها است.
فرمالدئید یک الکتروفیل قوی است. بنابراین در
واکنشهای جانشینی الکتروفیلی آروماتیک با ترکیبات آروماتیک شرکت میکند.
همچنین میتواند با آلکنها وارد واکنش افزایشی الکتروفیلی شود. در حضور
کاتالیزورهای بازی یک واکنش خود اکسایش - کاهش ( واکنش کانیزارو ) انجام
داده ، متانول و نمک اسید فرمیک تولید میکتد.
فرمالدئید بطور برگشت
پذیر پلیمریزه شده و تولید تریمر حلقهای 5 و 2 و 1 تری اکسان یا پلیمر
خطی پلی اکسی متیلن میکند. تشکیل این پلیمرها باعث میشود که رفتار گاز
فرمالدئید بطور اساسی از قانون گازهای ایدهآل انحراف داشته باشد، بخصوص در
فشار بالا یا دمای پائین ، فرمالدئید به آسانی با اکسیژن جَو اکسید شده و
تشکیل اسید فرمیک میدهد. برای جلوگیری از این واکنش ، محلول فرمالدئید
باید در بطریهایی با دربهای مهر و موم شده نگهداری شو
تولید فرمالدئید
فرمالدئید
در صنعت از اکسیداسیون کاتالیزوری متانول تهیه میشود. معمولا از نقره
فلزی یا مخلوط اکسید آهن و مولیبدن به عنوان کاتالیزور استفاده میشود. در
صورت استفاده از اکسید آهن و مولیبدن به عنوان کاتالیزور ، متانول با
اکسیژن در دمای 400 درجه سانتیگراد واکنش داده و طبق واکنش زیر فرمالدئید
تولید میکند:
CH3OH + 1,2O2 -----> HCHO + H2O
کاتالیزور
نقره معمولا در دمای حدود 650 درجه سانتیگراد استفاده میشود. در این
فرایند 2 واکنش ، همزمان انجام میشوند. واکنش اول که در بالا به آن اشاره
شد و واکنش دوم هیدروژن زدایی از متانول است:
CH3OH -----> HCHO + H2
کاربرد
از
فرمالدئید به علت از بین بردن بیشتر باکتریها بعنوان محلول ضدعفونی کننده
استفاده میشود. همچنین برای نگهداری از نمونههای بیولوژیکی هم مورد
استفاده قرار میگیرد. عمدهترین استفاده فرمالدئید در تولید پلیمر و سایر
ترکیبات شیمیایی است. رزینهای فرمالدئید ، از واکنش فرمالدئید با فنل ،
اوره و ملامین ایجاد میشوند. این مواد معمولا بعنوان رزینهای چسبناک در
تولید تختههای سهلایی ، در ساخت اسفنجهای قالبگیری شده و تولید اسفنجهای
عایق کاربرد دارند.
بیشتر از نصف فرمالدئید تولید شده صرف تولید
رزینهای فرمالدئید میشود. فرمالدئید در تولید مواد شیمیایی دیگر مانند
بسیاری از الکلهای چند عاملی مثل پنتا تریاول که در رنگسازی و تولید مواد
منفجره کاربرد دارد، استفاده میشود. از دیگر مشتقات فرمالدئید میتوان
دیفنیل متان را نام برد که در تهیه ترکیبات مهمی مثل پلیاوره تان که در
ساخت رنگ و فوم (اسفنج) کاربرد دارد و هگزا متیلن تترا آمین که در رزینهای
فنل فرمالدئید و ساخت مواد منفجره استفاده میشود.
نکات ایمنی
به
دلیل اینکه رزینهای فرمالدئید در ساخت بسیاری از مواد ، مانند تخته
سهلایی ، اسفنجهای افشانهای و فوم استفاده میشوند. این مواد در طول زمان
به آرامی فرمالدئید نشر میکنند. به این علت ، فرمالدئید یکی از مهمترین
آلایندههای هوای درون خانه است. غلظتهای بالای 0.1ppm آن در هوای خانه
باعث سوزش چشم ، آسیب به غشای مخاطی ، سر درد و احساس سوزش در نای و مشکل
شدن تنفس میشود. نوشیدن محلول فرمالدئید میتواند منجر به مرگ شود.
فرمالدئید در بدن به اسید فرمیک تبدیل شده ، با نفوذ به خون ، باعث بالا
رفتن اسیدیته آن میشود.
نفسهای تند و بریده ، بیهوشی ، کما و امکان مرگ
از علائم نوشیدن مقدار زیادی محلول فرمالدئید است. فرمالدئید در بدن
میتواند موجب ایجاد تغییر در پروتئینهای DNA شود. حیوانات آزمایشگاهی که
در معرض دوزهای بالای فرمالدئید قرار گرفتهاند، در طول زندگی خود به
سرطانهای پیشرفته در نای و گلو مبتلا شدهاند. با این همه برخی مطالعات
نشان میدهند که غلظتهای پایین فرمالدئید که کارگران کارخانههای تخته
سهلایی با آن مواجهاند، عامل سرطان زا نیست. اما فرمالدئید را در رده
سرطانزاهای احتمالی در انسان طبقهبندی میکنند.
